Anvisa facilita liberação de novas vacinas no Brasil
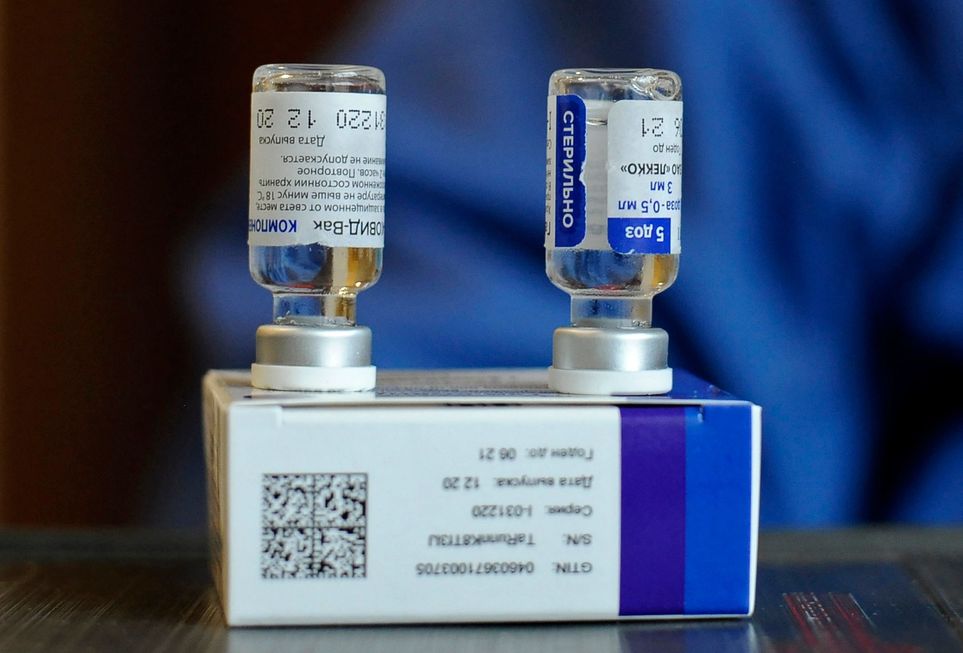 A vacina desenvolvida pelo Instituto Gamaleya, da Rússia, aparece como principal beneficiada pela nova medida. Crédito da foto: Jorge Bernal / AFP
A vacina desenvolvida pelo Instituto Gamaleya, da Rússia, aparece como principal beneficiada pela nova medida. Crédito da foto: Jorge Bernal / AFP
A Agência Nacional de Vigilância Sanitária (Anvisa) decidiu mudar regras para que empresas peçam o uso emergencial de vacinas para Covid-19 no Brasil, o que pode facilitar a entrada da Sputnik V. A agência informou ontem (3) que retirou a exigência de que estudos de fase 3 estejam em andamento no País para conceder este aval, passando a se valer de dados de estudos conduzidos internacionalmente. Pouco depois, porém, informou-se que a vacina indiana Covaxin pediu autorização para testes. E o Ministério da Saúde divulgou que negocia a compra de 30 milhões de doses de Sputnik V e Covaxin.
A Anvisa informou que o prazo para análise de uso emergencial nessas condições deverá ser de 30 dias. Para as vacinas com estudos nacionais, o prazo da agência foi de dez dias, como nos casos da Coronavac e do imunizante de Oxford/AstraZeneca, que obtiveram autorização em janeiro. A justificativa para o aumento do prazo é que, no caso dos estudos nacionais, houve acompanhamento mais próximo, o que facilitou a análise. Para os estudos conduzidos fora do País, será necessário analisar dados de pesquisas desde a fase inicial até o estágio mais avançado, que não tiveram acompanhamento prévio.
A discussão ocorre no momento em que a Anvisa é pressionada para liberar o uso do imunizante desenvolvido pelo Instituto Gamaleya, da Rússia. No Brasil, a União Química afirma que pode receber 10 milhões de doses prontas do imunizante até março. Além disso, entregar 150 milhões de unidades em 2021, somando a produção que seria feita no Brasil.
A retirada desta exigência também pode facilitar a entrada de outras vacinas no País. O laboratório indiano Bharat Biotech, por exemplo, já mostrou interesse em trazer a Covaxin ao setor público e privado brasileiro. A diretoria da Anvisa lembrou que o Brasil é elegível para receber diferentes vacinas pelo consórcio Covax Facility. Assim, a mudança na exigência da análise pode passar a englobar eventualmente imunizantes como o da Moderna e a Novavax.
A Sputnik V tem eficácia de 91,6% contra casos sintomáticos da covid-19. Os dados, avaliados por pesquisadores independentes, foram publicados na terça-feira (2) na revista científica The Lancet. A vacina já está sendo aplicada na Rússia e em outros países, como Argentina e Argélia.
Questionada sobre a motivação para a mudança nos critérios diante da aparente pressão pela Sputnik V, a diretora da Anvisa Meiruze Freitas disse que a alteração “não tem nada a ver com a decisão de publicação do Lancet, diria que foi coincidência”. “O processo está sendo discutido há mais tempo. Não foi pleito de nenhuma empresa, do governo, do Ministério da Saúde”, acrescentou. (Mateus Vargas e Marco Antônio Carvalho - Estadão Conteúdo)