Anvisa e Astrazeneca discutem uso emergencial
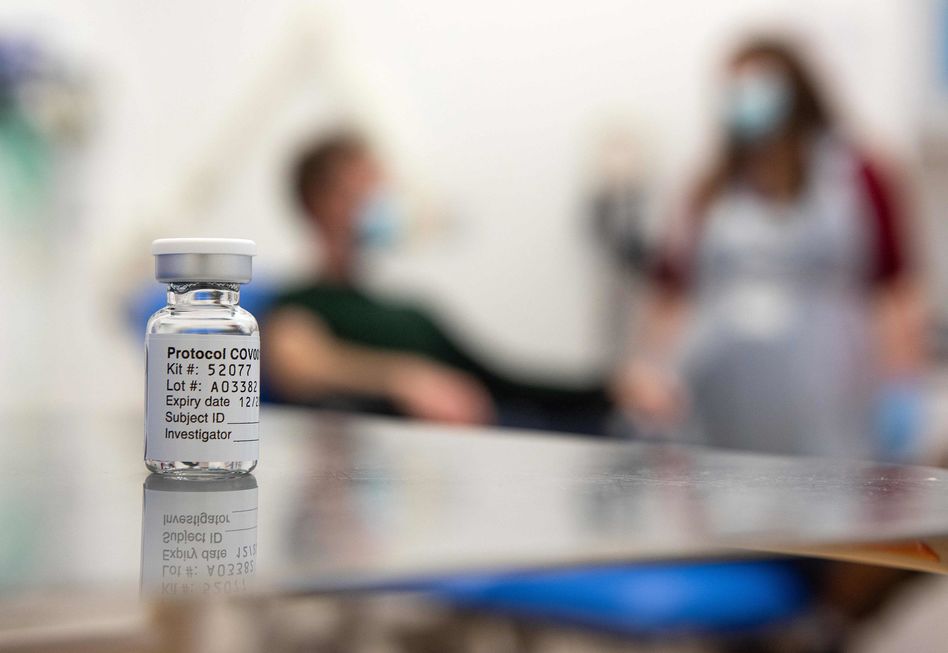 No Brasil a pesquisa é feita em parceria com a Fundação Oswaldo Cruz. Crédito da foto: AFP
No Brasil a pesquisa é feita em parceria com a Fundação Oswaldo Cruz. Crédito da foto: AFP
A Agência Nacional de Vigilância Sanitária (Anvisa) se reuniu ontem com representantes da Astrazeneca no Brasil para discutir previsão de pedido de uso emergencial da vacina contra a Covid-19 desenvolvida pela farmacêutica em parceria com a Universidade de Oxford. O imunizante, que recebeu autorização para uso emergencial no Reino Unido e Argentina ontem, é a principal aposta do governo brasileiro para vacinação da população. O imunizante teria eficácia de 70% com 21 dias após a 1ª dose.
Na reunião, ficou definido que o pedido de autorização para uso emergencial da vacina será feito pela Fundação Oswaldo Cruz (Fiocruz), que é o laboratório parceiro da farmacêutica no País. A Fiocruz deve pedir o registro à agência na próxima semana. O governo investiu R$ 1,9 bilhão para compra, processamento e distribuição de 100 milhões de doses do imunizante.
Segundo a Anvisa, o prazo de avaliação da solicitação é de até dez dias contados a partir da entrada do pedido formal, mas ele pode ser menor, tendo em vista que informações apresentadas na Submissão Contínua para registro serão consideradas. A medida, de acordo com a agência, é para evitar “o retrabalho” e promover “a otimização do processo”.
Até o momento, a Anvisa já participou de 48 reuniões com laboratórios com o intuito de dar orientações e fazer o acompanhamento dos imunizantes em desenvolvimento.
Argentina e Reino Unido
Um dia após começar a vacinação contra a Covid-19, com a russa Sputnik V, a Argentina autorizou, ontem, o uso do imunizante britânico desenvolvido pela farmacêutica Astrazeneca e a Universidade de Oxford. A liberação ocorreu poucas horas após o Reino Unidos anunciar a autorização da mesma vacina de forma emergencial.
“O produto mencionado apresenta um aceitável equilíbrio de benefício-risco, permitindo sustentar o consentimento da inscrição e da autorização do produto para a indicação solicitada”, diz resolução da Administração Nacional de Medicamentos, Alimentos e Tecnologia Médica (ANMAT, na sigla em espanhol).
A liberação tem validade de um ano. Há uma semana, a Argentina já havia liberado também a aplicação da vacina desenvolvida pela Pfizer e a Biontech, embora não tenha acordo ainda firmado com os responsáveis.
O governo argentino tem um convênio para a produção da vacina com a AstraZeneca, em uma aliança que também inclui o México. O imunizante, que pode ser mantido em refrigeradores, deve ser adquirido por cerca de US$ 2,50, por dose. O País também planeja fabricar 3 milhões de doses em 2021.
Pandemia no Brasil
O total de mortes provocadas pela pandemia no novo coronavírus no Brasil chegou a 193.875. Nas últimas 24 horas, as autoridades sanitárias registraram 1.194 novos óbitos. Há ainda 2.488 óbitos em investigação.
Este foi o segundo dia consecutivo com o registro de novas mortes acima de mil vítimas. Na terça-feira, foram acrescidos 1.111 novos óbitos às estatísticas. A última vez que o número de novos registros em 24 horas havia passado das 1.190 mortes foi em 1º de setembro, quando foram confirmados 1.215 novos óbitos. O total de pessoas infectadas desde o início da pandemia atingiu 7.619.200. (Da Redação, com informações de Estadão Conteúdo e Agência Brasil)